|
pH Wert Überwachung
mit ESP32
Bevor man mit der Messung beginnen kann muss man als erstes den
Messbereich mit dem Potentiometer einstellen (0 - 3.3 V). Damit man
nicht im negativen Messbereich misst, wird der Nullpunkt (also pH =
7) auf 2,5 V eingestellt.
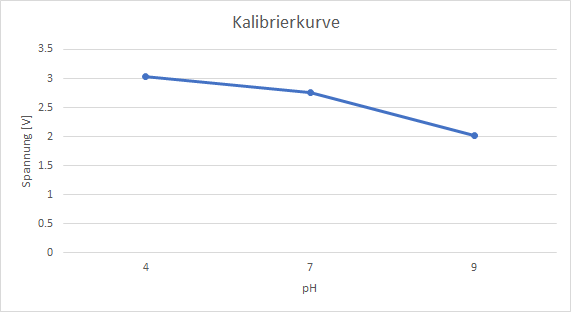
Die Kalibrierung erfolgt durch eine Kalibrierkurve mithilfe der
Kalibrierlösungen pH4 (rot), pH7 (grün) und pH9 (blau). Die pH-Elektrode OPF32 von der Firma IKS wurde
hierbei verwendet. Folgende Werte wurden für die Kalibrierung
gemessen:

Kalibrierung pH4

Kalibrierung pH7

Kalibrierung pH9

Messaufbau
|
|
voltage [V] |
pH |
pH/V |
|
Pufferlösung pH 4 |
3.03 |
4 |
1.32013201 |
|
Pufferlösung pH 7 |
2.76 |
7 |
2.53623188 |
|
Pufferlösung pH 9 |
2.02 |
9 |
4.45544554 |
|